药厂微生物监控很重要吗? 需要鉴定每一株菌吗?
发布时间:2022-08-22 浏览次数:2548
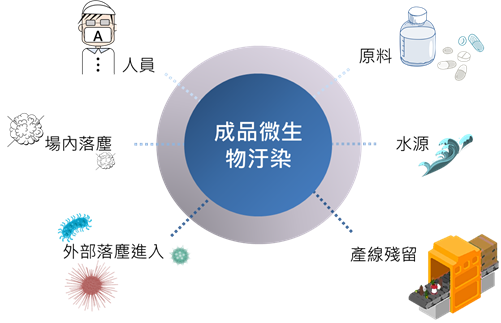
药厂的微生物监控,要从法规开始谈起
大家都知菌种鉴定是药厂微生物监控不可或缺的一环,难道需要监控到一颗菌株都不能出现才算合格吗?
依据USP<1113>(美国药典法第1113章节)的规范,微生物监控的重要性是在于:在药品的制造生产过程中,一旦侦测到菌,必须对其特征/特性有所了解,包括鉴定和菌株分型,进而得知他对成品的危害程度大小。
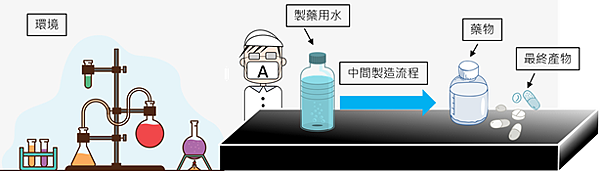
此外,当执行完整的灭菌步骤后,若仍有受菌污染的状况发生,此时进行菌种鉴定是很重要的。
不同条件的制造厂有不同规范标准
USP<62>(美国药典微生物鉴定第62章节)指出,对于不需无菌条件生产产品的制造厂,只需进行特定微生物(致病菌)的测试。
实验上,只需在选择性培养基或诊断性培养基上生长且表现出特定型态的菌株进行鉴定需求。
对于需无菌条件生产的药厂,USP <71>(美国药典微生物鉴定章节第71章节)提及,若厂内近性标准灭菌流程后,进行无菌测试结果中,仍长出的细菌,可藉由菌种鉴定了解它的特性,从而发现灭菌的材料或技术有什么问题。
USP <1113>(美国药典微生物鉴定章节第1113章节)叙述中提及:选择可鉴定到strain-level的鉴定系统,对于污染源的溯源追踪较合适。
药厂洁净等级划分ABCD级法规要求
洁净区域之空气等级及微生物品质如下表:
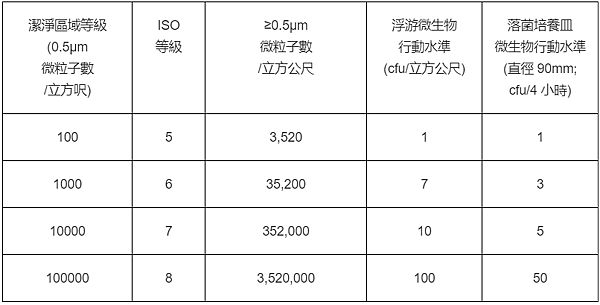
空气等级(国际医药品稽查协约组织药品优良制造准则, PIC/S):
| 静态 | 动态 | |||
| 等级 | 微粒最大允许量/立方公尺 | |||
| ≥0.5μm | ≥5μm | ≥0.5μm | ≥5μm | |
| A | 3,500 | 1 | 3,500 | 1 |
| B | 3,500 | 1 | 350,000 | 2,000 |
| C | 350,000 | 2,000 | 3,500,000 | 20,000 |
| D | 3,500,000 | 20,000 | 未界定 | 未界定 |
ISO等级5的微粒浓度相等于100级,和欧盟分类的A级洁净区规范相等。
正常情况下,ISO等级5(A级洁净区)环境等级区的样本,应无微生物生长。
A级洁净区:通常为药厂高风险无菌操作区域。
B级洁净区:通常为和A级区相连的走道或区间。
C 、D级洁净区:无菌要求等级较低的区域,对于菌量的容忍度较高,但不可超标。
USP <1116> 美国药典微生物鉴定章节<1116>针对分离菌株的微生物鉴定:
♦ 成功的环境控制须对于所获取到的微生物菌群进行适当比例的鉴定。
♦ 菌种鉴定的资讯收集对于调查污染源,尤其是超过环境安全等级规范数量有很大的帮助。
♦ 关键和紧邻区域的微生物鉴定应优先于非关键区域的微生物鉴定。






